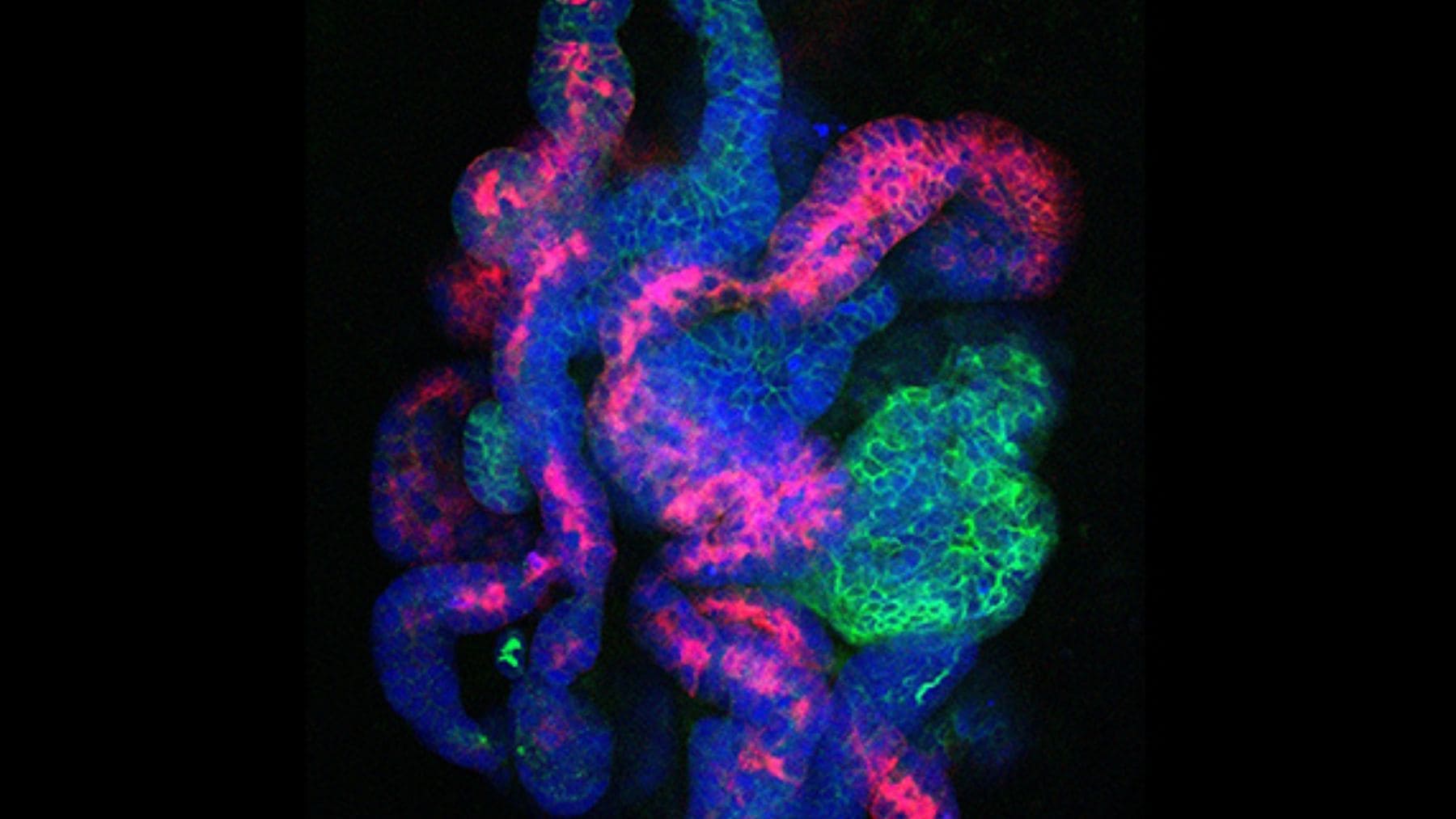
Imagina estudiar una enfermedad del riñón no en animales ni en placas de plástico, sino en un riñón en miniatura cultivado en la mesa del laboratorio. Eso es lo que ha logrado un equipo de la Universidad del Sur de California al crear pequeños riñones artificiales a partir de células madre humanas y de ratón. El trabajo acerca la idea de fabricar tejidos de reemplazo y de probar fármacos directamente sobre versiones en 3D del órgano.
Los científicos han conseguido que unas células clave del riñón llamadas células progenitoras de nefrona se mantengan jóvenes y se multipliquen durante meses en el laboratorio. Mediante cambios precisos en dos proteínas de señalización llamadas p38 y YAP estas células forman organoides renales en 3D que imitan partes de un riñón real e incluyen filtros de alta precisión. Incluso han visto que ciertas células maduras pueden volver atrás hasta un estado parecido al de estas células progenitoras lo que sugiere una capacidad de regeneración más flexible de lo que se pensaba.
Qué hace realmente un riñón y qué son las nefronas
Cada riñón humano está formado por cientos de miles de nefronas que son las unidades de filtrado que limpian la sangre y forman la orina. Cada nefrona actúa como una pequeña planta depuradora que decide qué se queda en el cuerpo y qué se va al inodoro. Cuando fallan demasiadas nefronas la persona por lo general necesita diálisis o un trasplante.
En el desarrollo embrionario las nefronas nacen a partir de las llamadas células progenitoras de nefrona abreviadas NPC en inglés que funcionan como el molde del que salen todas las piezas. Otra pieza clave son los podocitos que forman parte del filtro fino que retiene proteínas útiles mientras deja pasar los desechos y su comportamiento está ligado a muchas enfermedades renales congénitas y a ciertos tipos de cáncer. Una investigación previa del laboratorio de Li ya mostró otros organoides renales y el nuevo trabajo completa en gran medida el mapa al centrarse en las NPC que generan las nefronas.
Cómo han creado los mini riñones en la Universidad del Sur de California
El nuevo estudio de 2024 del grupo de Li está liderado por Zhongwei Li en elUSC UKRO Kidney Research Center con primera autoría de Biao Huang. El equipo ha desarrollado un sistema de cultivo químicamente definido que mantiene vivas y en expansión las NPC humanas y de ratón durante largos periodos al tiempo que conservan sus rasgos de célula progenitora. Según los autores las NPC generadas se parecen en gran medida a las células progenitoras humanas del riñón aisladas directamente de tejido real.
A partir de estas NPC los investigadores produjeron organoides renales pequeños riñones tridimensionales con múltiples tipos celulares organizados. Estos organoides muestran podocitos más maduros y menos células fuera de lugar que los modelos de riñón en miniatura anteriores lo que mejora la fidelidad del modelo para estudiar cómo funciona el órgano. Además el cultivo reveló que ciertos podocitos humanos pueden reprogramarse de nuevo a un estado similar al de una NPC lo que apunta a una plasticidad inesperada en el tejido renal.
Un nuevo modelo para fármacos y terapias de reemplazo renal
¿Qué se puede hacer con un mini riñón tan realista además de mirarlo al microscopio? Disponer de NPC que se expanden bien en placas de laboratorio abre la puerta a algo más que fabricar organoides bonitos porque las líneas celulares estables permiten aplicar pantallas de edición genética a gran escala como las basadas en CRISPR para identificar genes implicados en el desarrollo del riñón y en enfermedades hereditarias. En este trabajo el grupo de Li también modeló una forma común de enfermedad hereditaria llamada poliquistosis renal autosómica dominante y encontró compuestos que reducen la formación de quistes en los mini riñones.
Como resume Li “al mejorar nuestra capacidad de cultivar NPC a partir de células madre humanas creamos una nueva vía para comprender y combatir las enfermedades renales congénitas y el cáncer”. Según el propio equipo este avance tiene el potencial de impulsar la investigación renal desde acelerar el descubrimiento de fármacos hasta desentrañar en gran medida las bases genéticas del desarrollo la enfermedad y el cáncer renales. Para quienes viven pendientes de una máquina de diálisis todo esto suena aún lejano pero al final del día lo que intenta hacer esta línea de trabajo es preparar el terreno para futuros riñones sintéticos y terapias de reemplazo más seguras.
El estudio principal se ha publicado en la revista Cell Stem Cell.